Weiterführende Informationen
- PSA bei der Prostatakarzinom-Früherkennung
- Fusionsbiopsie der Prostata
- Prostataentfernung bei Prostatakrebs
- Perkutane Strahlentherapie bei Prostatakarzinom
- Brachytherapie bei Prostatakrebs
- Androgendeprivations-Therapie (ADT) beim Prostatakarzinom
- Therapie mit Enzalutamid, Apalutamid, Darolutamid und Abirateron beim Prostatakarzinom
- Chemotherapie bei Prostatakarzinom
- Therapie mit PARP-Inhibitoren
- Knochenprotektion bei Prostatakarzinom
- Radioligandentherapie (RLT) bei Prostatakarzinom
- Chemotherapie bei urologischen Erkrankungen
- Prostatabiopsie
Mit über 60.000 Neuerkrankungen und etwa 15.000 Todesfällen pro Jahr ist der Prostatakrebs in Deutschland die häufigste Krebserkrankung bei Männern. Früh erkannt ist dieser Tumor in 80 bis 90 Prozent der Fälle heilbar. Die Ursachen sind im Wesentlichen unbekannt. Relevante Faktoren sind vor allem das Alter und das männliche Hormon Testosteron, da der Tumor hormonabhängig wächst. Eine familiäre Häufung des Prostatakrebses ist inzwischen als Risikofaktor belegt, ebenso das erhöhte Risiko bei afroamerikanischen Männern. Zudem könnten chronische Entzündungen der Prostata und sexuell übertragbare Erkrankungen
möglicherweise das Prostatakrebs-Risiko vermehren. Einflüsse durch hohen Alkoholkonsum, durch tierische Fette oder erhöhten Fleischkonsum werden vermutet. Normalgewicht und ausreichende Bewegung könnten das Risiko für einen Prostatakrebs verringern.
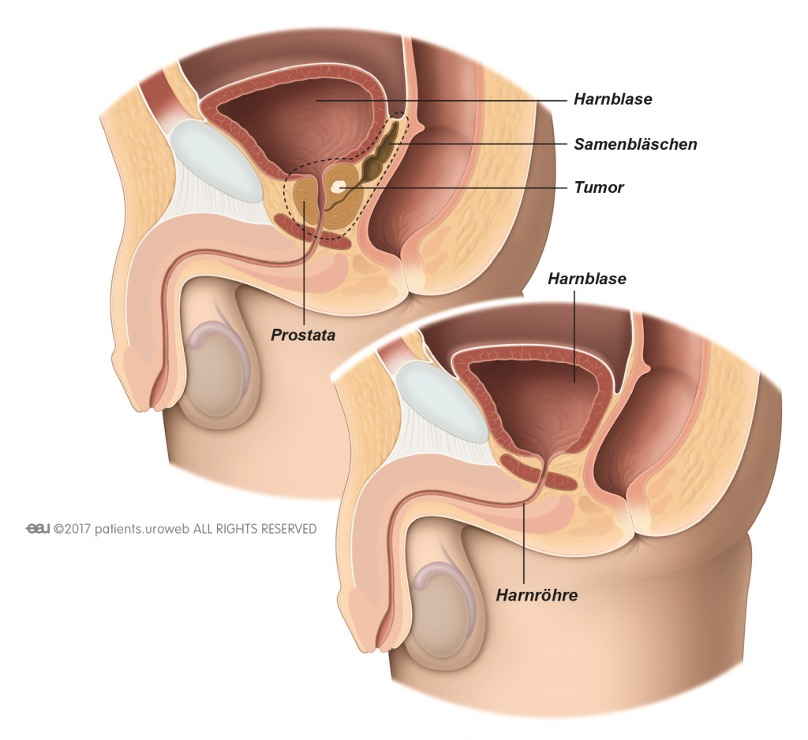
Fakten zum Prostatakarzinom
Krebsart: Das Prostatakarzinom im engeren Sinn, das in diesem Beitrag besprochen wird, entwickelt sich aus dem Drüsengewebe in der Prostata und ist damit ein Drüsenkrebs (Adenokarzinom). Darüber hinaus gibt es in der Prostata selten weitere Krebsarten auf dem Boden anderer Gewebsstrukturen, beispielsweise intraductale Karzinome, die hier nicht Thema sind.
Ausbreitung: In der Prostata kann der Krebs als einzelner Herd auftreten, häufig finden sich aber mehrere Krebsareale in verschiedenen Regionen des Organs, die jeweils auch von unterschiedlicher Aggressivität sein können. Wenn diese Krebsherde die Grenzen der Prostata nicht überschritten haben, spricht man von einem lokal begrenzten Prostatakrebs. Wenn der Tumor über die Grenzen der Prostata hinausgeht, kann er dies entweder örtlich begrenzt tun und nur angrenzende Gewebsbereiche betreffen (T3-Tumor) oderkann zusätzlich Lymphknoten in der Nähe der Prostata betreffen (N+) (lokal fortgeschrittener Tumor).Der Prostatakrebs kann aber auch zu Metastasen in entfernt liegenden Lymphknoten oder Organen, meist in den Knochen führen (metastasierter Tumor).
Wachstumsgeschwindigkeit: Das Prostatakarzinom ist grundsätzlich ein eher langsam wachsender Tumor mit einer Entwicklungszeit über Jahre, bis es zu Metastasen oder Beschwerden führt oder lebensbedrohlich wird. Deutlich seltener gibt es auch Unterformen des Prostatakrebses, die schnell wachsen und früh zu Metastasen führen. Dies hat Konsequenzen für z.B. Früherkennungsmaßnahmen, weil auch aus ärztlicher Sicht nur solche Krebse festgestellt werden sollten, die den Patienten mit großer Wahrscheinlichkeit schädigen oder zu seinem Tod führen. So rät die deutsche S3-Leitlinie zum Prostatakarzinom denjenigen Patienten von einer Früherkennung ab, deren Lebenserwartung unter 10 Jahren liegt. Damit soll eine Überdiagnostik und Übertherapie vermieden wegen
Testosteron und Prostatakrebszelle: im Prinzip wird die Entwicklung und Vermehrung von Prostatakrebszellen durch Testosteron, dem körpereigenen männlichen Geschlechtshormon, gefördert, unter dessen Einfluss ein Prostatakrebs wächst. Umgekehrt wissen wir, dass sich ein Prostatakrebs nicht weiterentwickelt oder sogar zurückbildet, wenn er durch eine Behandlung dem Einfluss dieses Hormons entzogen wird. In dieser Phase der Tumorentwicklung spricht man von einem hormonsensitiven Tumor, und er kann erfolgreich mit einer Hormon-Entzugstherapie behandelt werden.
Allerdings kann der Krebs im Verlauf diese Eigenschaft verlieren und nicht mehr auf diese Form der Therapie ansprechen. In dieser Krankheitsphase wird er als hormonunabhängig bezeichnet, und es müssen andere Behandlungsmethoden angewandt werden.
Symptome und Früherkennung von Prostatakrebs
Der Prostatakrebs verursacht zunächst keine Symptome. Deshalb ist die Frühform eines Prostatakrebses nur durch ärztliche Untersuchungen zu erkennen. Beschwerden treten häufig erst in fortgeschrittenen Stadien auf, z. B. durch eine Einengung der Harnröhre oder durch Metastasen (z. B. Knochenschmerzen).
Das gesetzliche Krebsfrüherkennungsprogramm in Deutschland umfasst derzeit für Männer ab 45 Jahren einmal jährlich neben der Abklärung von Beschwerden die Untersuchung der äußeren Geschlechtsorgane sowie die Tastuntersuchung der Prostata und der Lymphknoten. Der PSA-Test im Blut ist zwar für Patienten mit Wunsch nach einer Früherkennungsuntersuchung klar von der Leitlinie empfohlen, ist aktuell aber nicht Bestandteil der gesetzlichen Früherkennung und muss vom Patienten selbst getragen werden, wenn nicht schon der konkrete Verdacht auf einen Prostatakrebs bestünde.
Bevor Sie sich für eine Früherkennungsuntersuchung auf Prostatakrebs entscheiden, sollten Sie Nutzen und Risiken gemeinsam mit Ihrem Urologen oder Ihrer Urologin abwägen, denn durch Früherkennungsuntersuchungen können auch Prostatakrebserkrankungen entdeckt werden, die keiner Behandlung bedürfen. Denn diese führen insbesondere in höherem Lebensalter zu keiner Verkürzung der Lebenszeit oder Beeinträchtigung der Lebensqualität. Diese Überlegung gilt entsprechend auch für die Bestimmung des PSA-Wertes.
Früherkennungsoptionen und PSA-Test
Expertenkonsens ist, dass Männern, die nach ausführlicher und ergebnisoffener Beratung eine Früherkennungsuntersuchung wünschen, eine Bestimmung des PSA-Wertes angeboten wird. Je nach Befund und Risikokonstellation wird weiterführend eine Kernspintomografie empfohlen, einer mulitparametrische MRT der Prostata (mp-Prostata-MRT). Männer ab dem 45. Lebensjahr mit einer mutmaßlichen Lebenserwartung von mehr als zehn Jahren sollten über die Möglichkeit einer solchen Früherkennung informiert werden. Bei Männern, die ein möglicherweise erhöhtes Erkrankungsrisiko (z.B. Prostatakrebserkrankung des Vaters, Erkrankung des Bruders) tragen, kann die Altersgrenze um fünf Jahre vorverlegt werden.
Einen Hinweis auf einen Prostatakrebs kann auch die Tastuntersuchung vom After geben, wenn dabei ein Knoten zu tasten ist. Diese, aktuell von den gesetztlichen Krankenkassen noch einzige bezahlte Untersuchung für die Früherkennung, kann nur in sehr wenigen Fällen eine Prostatakrebserkrankung im Frühstadium diagnostizieren und verliert daher in der Früherkennung zunehmend an Bedeutung und wird aktuell hierfür von der Leitlinie nicht mehr empfohlen, hat jedoch noch seinen Stellenwert zur Beurteilung anderer Prostataerkrankungen oder bei bereits diagnostiziertem Prostatakrebs. .
Der PSA-Wert ist ein Eiweiß aus der Prostata, das bei jedem Mann im Blut nachgewiesen werden kann. Seine Höhe und ansteigende Werte können Verdachtsmomente für das Vorliegen eines Prostatakrebses sein. Allerdings gibt es keine typischen Normalwerte wie bei anderen Laborbefunden, sondern es wurden Grenzwerte (sogenannte cut-off-Werte) festgelegt. Aktuell wird ein Wert über 3 ng/ml zunächst als potentiell verdächtig angesehen.
Ist der PSA-Wert bei einer Untersuchung verdächtig erhöht, sollte er zunächst nach wenigen Wochen im gleichen Labor und mit derselben Methode kontrolliert werden.
Allerdings werden diese Grenzwerte darüber hinaus abhängig vom Alter und von der Prostatagröße unterschiedlich bewertet, da der PSA-Wert auch beim Gesunden mit dem Alter und mit der Prostatagröße ansteigt. Auch kann der PSA-Wert beispielsweise durch eine Harnwegs- oder Prostataentzündung vorübergehend ansteigen. Damit sind diese Grenzwerte nur eine grobe Orientierung und eine Risikostratifizierung unter Berücksichtigung individueller Faktoren ist notwendig.
Lesen Sie auf unserer Seite mehr zum Thema:
Zukunftspläne: Wie dargestellt besteht eine Diskrepanz der Leitlinienempfehlung und der aktuell von den Krankenkassen übernommenen Untersuchung für die Früherkennung. Die aktuellen Studiendaten und damit die Leitlinie empfehlen, auf die rektale Untersuchung, also die Tastuntersuchung vom After, komplett zu verzichten und den PSA-Wert in das Zentrum der Früherkennung zu stellen. Ebenso wir eine mpMRT der Prostata nicht regelhaft von den gesetzlichen Krankenkassen übernommen. Es ist zu hoffen, dass diese neuen Erkenntnisse auch von medizinpolitischer Seite in den Leistungskatalog der Krankenkassen eingeführt werden, Üblicherweise dauert dieser Prozess aber mehrere Jahre, sodass aktuell die Diskrepanz zwischen Leitlinienempfehlung und Kostenerstattun besteht.
Diagnostik
Basisuntersuchungen
Die ausführliche Erhebung der medizinischen Vorgeschichte einschließlich der Familienvorgeschichte ist stets der Beginn eines Untersuchungsgangs.
Die körperliche Untersuchung schließt die Flanken, den Bauch, das Genitale, Lymphknotenstationen und fakultativ die rektale Untersuchung ein. Bei ihr werden vom After aus die Prostata und der Enddarm betastet.
Die Urinuntersuchung informiert unter anderem über mögliche Harnwegsinfektionen.
Mit Ultraschall können die Nieren, die Blase und die Prostata vom Bauch aus beurteilt werden. Bei der transrektalen Sonografie wird eine dünne Ultraschallsonde in den After eingeführt, die eine detailliertere Beurteilung der Prostata erlaubt. Beide Untersuchungen sind nicht zwingend Teil der Vorsorge.
Bei Laboruntersuchungen stehen der PSA-Wert und die Nierenfunktionswerte im Mittelpunkt.
Zusätzlich sollte bei auffälligen Befunden oder Risikokonstellationen frühzeitig ein multiparametrisches Prostata-MRT (mpMRT) erfolgen, bevor eine Biopsie durchgeführt wird.
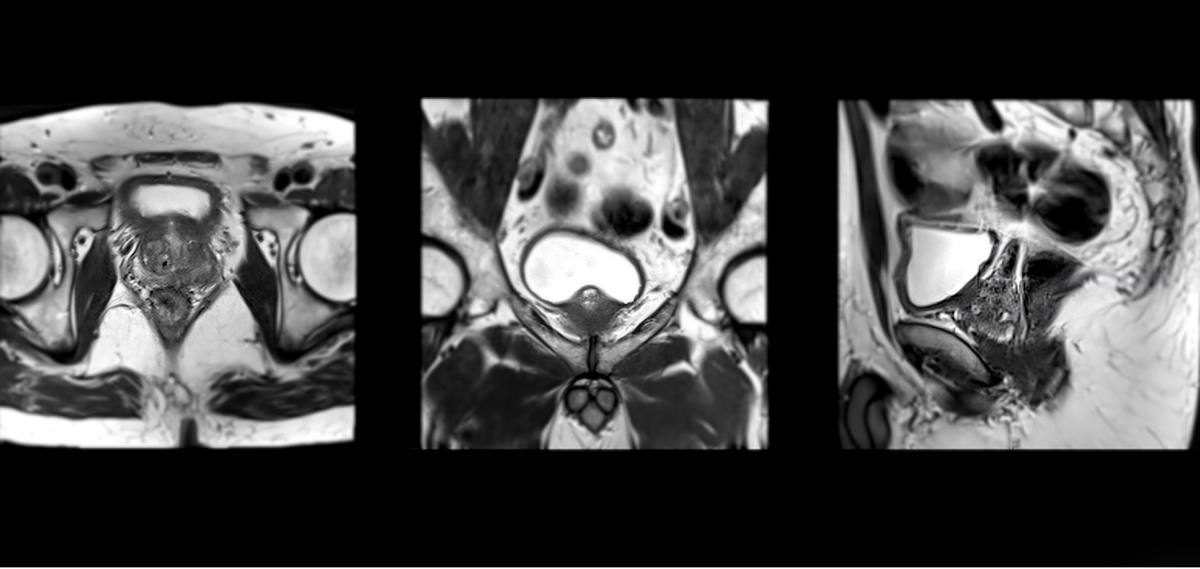
Multiparametrisches Prostata-MRT
Die multiparametrische MRT (mpMRT) der Prostata ist eine moderne, schmerzfreie Bildgebungsmethode zur genauen Untersuchung der Prostata. Sie kombiniert verschiedene MRT-Techniken, um Gewebeveränderungen sichtbar zu machen. Die Untersuchung dauert in der Regel 30 bis 45 Minuten und erfolgt in Rückenlage in einem MRT-Gerät. Für die Wahrscheinlichkeit für das Vorliegen eines Prostatakrebs wird für jeden einzelnen Sektor ein sog. PI-RADS-Wert angegeben. Im Ergebnis entsteht dabei ein Bild der Prostata, auf dem diejenigen ihrer Anteile abgrenzbar sind, in denen ein Krebsverdacht besteht. Ein PI-RADS-Wert ≥3 gilt dabei als potentiell verdächtig.
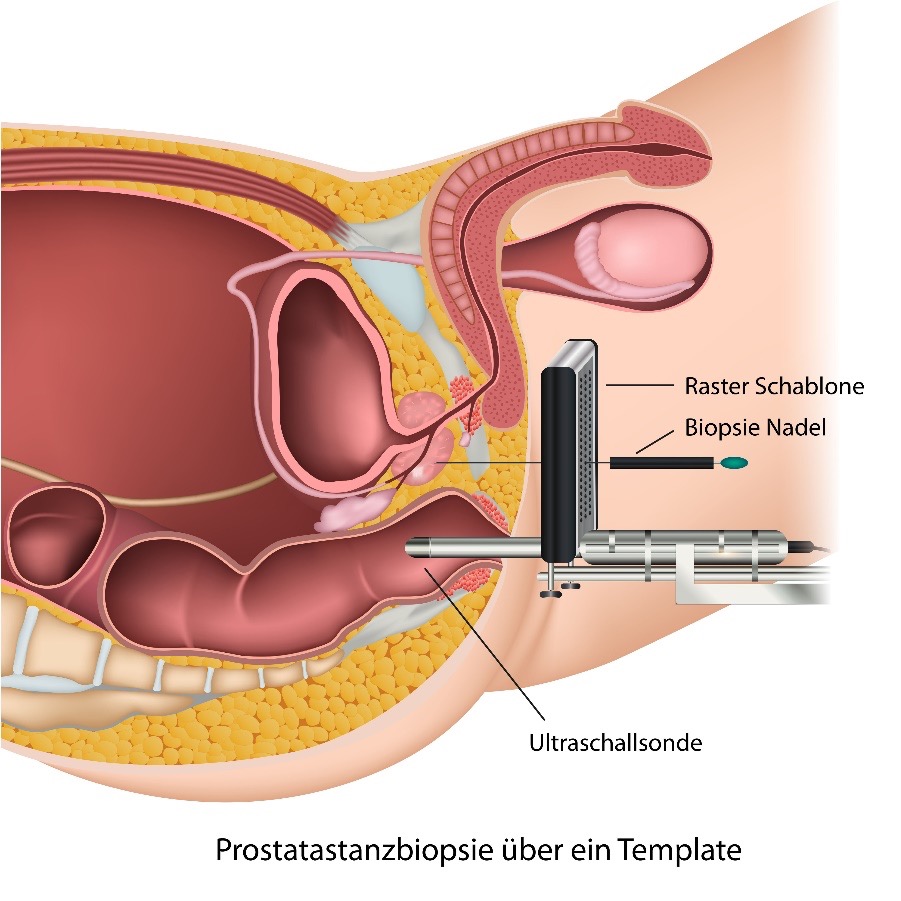
Probenentnahme (Prostatabiopsie)
Ergibt sich aufgrund des PSA-Werts,der MRT-Befunde oder der Tastuntersuchung der Verdacht auf einen Prostatakrebs, werden bei einer sogenannten Prostatabiopsie mit einer dünnen Nadel Gewebeproben aus der Prostata entnommen. Die Proben können entweder durch den After (transrektal) oder vom Damm aus, also zwischen After und Hodensack (perineal), entnommen werden. Die Probenentnahme wird gesteuert mit transrektalem Ultraschall (TRUS-gesteuerte Biopsie), der mit einer dünnen Sonde im After durchgeführt wird. Bei der Fusionsbiopsie werden in Echtzeit die Ergebnisse des multiparametrischen Prostata-MRT mit den Bildern des Ultraschalls überlagert, so dass ein gezielteres Vorgehen möglich ist. Unter Ultraschallsteuerung werden dabei in der Regel systematisch 10 – 12 Proben aus den verschiedenen Teilen der Prostata genommen, so dass damit alle Bereiche der Prostata untersucht werden. Wurden im mpMRT tumorverdächtige Bereiche erkannt oder im Ultraschall, werden aus diesen zusätzlich gezielten Proben entnommen.
Lesen Sie auf unserer Seite mehr zum Thema:
Feingewebliche Untersuchung (Histologie)
Dabei wird im Labor von einem Pathologen unter dem Mikroskop untersucht, ob sich Krebszellen in diesen Proben befinden und wie aggressiv sie sind.
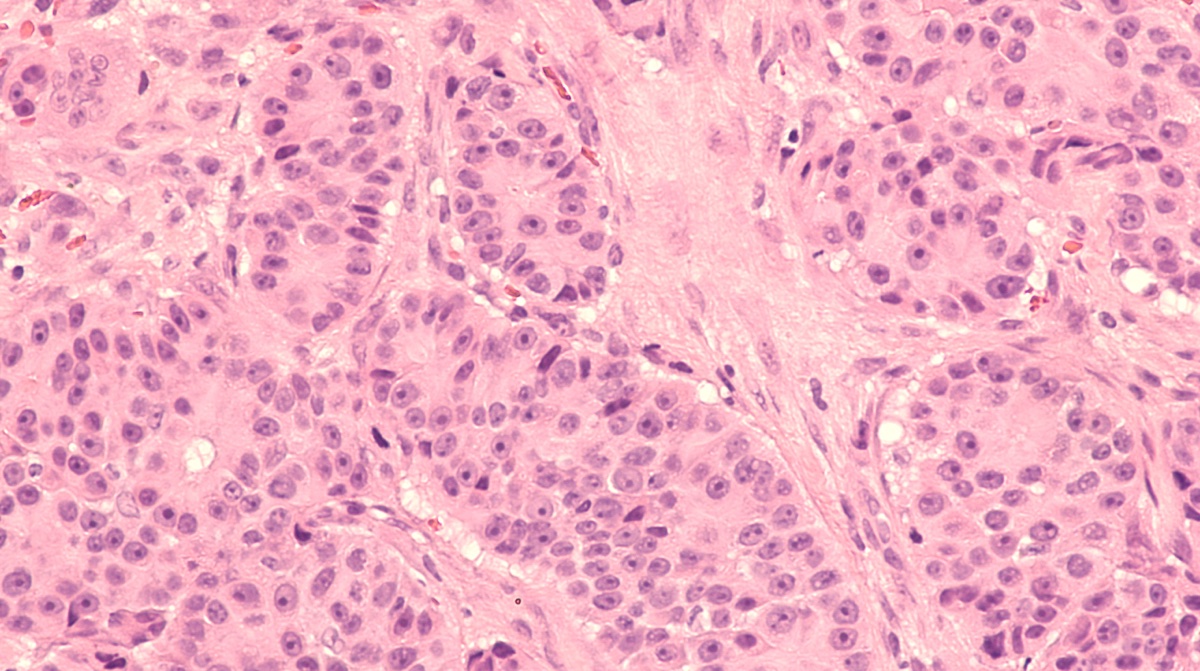
Zur Klassifikation der Veränderungen wird der sogenannte Gleason-Score verwendet. An mindestens zwei befallenen Proben werden die Zellveränderungen in Grade zwischen 1 (harmlos) und 5 (aggressiv) eingeteilt. Diese beiden Kennzahlen werden mit einem Pluszeichen verbunden. Findet sich beispielsweise in der einen Probe ein Gleason-Wert von 3 und in der anderen ein Wert von 4, wird der Gesamt-Gleason-Wert mit 3 + 4 beschrieben. Dabei wird die Kennzahl des am häufigsten gefundenen Anteils an die erste Position geschrieben, die des selteneren an die zweite. In unserem Beispiel wurde also häufiger ein Gleason-Wert von 3 und seltener ein Wert von 4 gefunden.
Die Aggressivität eines Tumors erhöht sich mit steigendem Zahlenwert. Ein Gleason-Score von 3 + 3 weist auf einen langsam wachsenden, ein Wert von 5 + 5 auf einen schnellwachsenden aggressiven Krebs hin.
Eine weitere Einteilung ist das ISUP-Grading-System mit den Graden 1–5, das die Aussagekraft des Gleason-Scores noch verbessert. Dabei steht die Zahl 1 für eine wenig, die Zahl 5 für eine hoch-aggressive Krebsform.
Bildgebende Diagnostik
Sowohl bei der Diagnosestellung wie auch im Krankheitsverlauf bringen bildgebende Untersuchungen mehr Informationen über den konkreten Zustand der Erkrankung. Das sind im Wesentlichen:
- Die Computertomografie, also eine Schnittbilduntersuchung von Becken und ggf. Bauch zur Beurteilung von Knochen- und Weichteilabsiedlungen
- Das Skelettszintigramm, bei dem eine radioaktive Substanz, die sich über die Blutbahn verteilt, alle Knochen darstellt und Knochenmetastasen anzeigt
- PSMA-PET-CT: bei dieser Untersuchung wird eine schwach radioaktive Substanz an einen Trägerstoff gekoppelt, der PSMA (Prostataspezifisches Membranantigen) enthält. Nach der Injektion bindet sich diese Kombination an die Wand der Prostata(krebs)zellen und reichert sich damit gezielt in den tumorbefallenen Bereichen an. Daraus entsteht das Bild des Körpers, in dem die Metastasen dargestellt werden (PET). Durch die Kombination der Untersuchung mit einem Computertomogramm (CT) lassen sich die Metastasen präzise den Körperbereichen und Organen zuordnen.
Der Zeitpunkt und die Auswahl dieser Untersuchungen orientieren sich an verschiedenen Kriterien. Dazu gehören die Aggressivität des nachgewiesenen Tumors, die bisherige Ausbreitung des Tumors, der Verlauf des PSA-Werts, der Krankheitsverlauf insgesamt und auch Beschwerden des Patienten. Die S3-Leitlinie empfiehlt das PSMA-PET-CT bevorzugt bei Hochrisiko-Tumoren und bei Rezidivverdacht zur Metastasensuche.
Stadieneinteilung
Aus diesen Untersuchungen ergeben sich die Stadieneinteilung des Prostatakrebses und eine „Tumorformel“, die auf einen Blick die Eigenschaften des Krebses beschreibt.
Die Stadien werden mit Zahlen (0 – 4) und Kleinbuchstaben (a – c) präzisiert, wobei ein höherer Wert einen größeren Umfang beschreibt. Gibt es zu einem Kriterium keine Information, wird der Kleinbuchstabe x eingesetzt
Es werden folgende Stadientypen unterschieden:
- T-Stadium: beschreibt das Ausmaß des Tumors in der Prostata
- N-Stadium: beschreibt das Ausmaß von Metastasen in den zugehörigen Lymphknoten
- M-Stadium: beschreibt Organmetastasen und Metastasen in entfernt liegenden Lymphknoten
Zusätzlich enthält die „Tumorformel“ die Angabe des Gleason-Scores und des PSA-Werts bei Diagnosestellung.
Die Angabe: „T1c N0 M0 Gleason 3 + 4 PSA 6,7 ng/ml“ beschreibt einen Tumor, der lediglich bei einer Biopsie festgestellt wurde, bei dem keine Lymphknoten- oder Organmetastasen festgestellt wurden, der nur mäßig aggressiv ist und der bei einem vergleichsweise niedrigen PSA-Wert festgestellt wurde.
Die Behandlung von Prostatakrebs
Wichtig ist zunächst die Frage, ob ein Tumor geheilt werden kann. Das ist meist der Fall, wenn er auf die Prostata begrenzt ist, denn dann bleiben verschiedene Methoden der Operation oder der lokalen Bestrahlung, die den Tumor heilen können. Hat der Tumor die Grenzen der Prostata überschritten, sinken die Chancen einer Heilung.
Liegt bereits eine Fernmetastasierung vor ist eine Heilung in der Regel nicht mehr möglich In diesen Fällen stellt die medikamentöse Behandlung die Haupttherapie dar, die eine gute Wirksamkeit gegen das Tumorleiden hat.
Generell ist wichtig zu wissen, dass die unterschiedlichen Behandlungsformen nur in bestimmten Phasen des Krankheitsverlaufs sinnvoll und auch nur dann zugelassen sind. Die Auswahl der Behandlung richtet sich nach Tumorstadium, Risiko, Alter, Begleiterkrankungen und Patientenwunsch.
Behandlung im Frühstadium
Wird ein Prostatakrebs so rechtzeitig gefunden, dass noch keine Metastasen vorliegen, kann dem Patienten Heilung in Aussicht gestellt werden, wenn die geeignete Behandlungsmethode gewählt wird. Dazu zählen:
Aktive Überwachung (Active Surveillance)
Bei einem Niedrigrisiko Prostatakarzinomen (in der Regel definiert als Gleason 3+3 und PSA <10-15 ng/ml) soll zunächst eine abwartende Strategie verfolgt werden, eine so genannte aktive Überwachung des Porstatakarzinoms (Active Surveillance), welche regelmäßige PSA-, MRT- und Biopsieuntersuchungen beinhaltet. Dieses Vorgehen basiert auf langjährigen Untersuchungen, die belegen konnten, dass das Risiko für eine Metastasierung in diesem Tumorstadium sehr gering sind. Die Kontroll-Untersuchungen dienen dazu, eine mögliche Veränderung des Tumors rechtzeitig zu detektieren, um in diesen Fällen dann eine aktive Therapie (s. folgende) einzuleiten. Dieses Vorgehen setzt allerdings neben einem Niedrigrisiko-Prostatakarzinom auch einen kooperativen Patienten voraus, der zu den konsequenten regelmäßigen Kontrolluntersuchungen einschließlich erneuter Prostatabiopsien bereit ist.
Operation
Eine wichtige Säule der Behandlung im lokalisierten und behandlungswürdigen Stadium eines Prostatakrebses ist die Komplettentfernung der Prostata, die radikale Prostatektomie. Dabei wird die Prostata mit den Bläschendrüsen entfernt, einschließlich des Teils der Harnröhre, der innerhalb der Prostata verläuft. Diese prostatische Harnröhre wird am Blasenauslass zur Harnröhre hin und knapp oberhalb des äußeren Schließmuskels durchtrennt. Die dadurch verursachten Öffnungen am Blasenauslass und in der Harnröhre werden mit Nähten sorgfältig vereinigt, so dass die Harnröhre wieder kontinuierlich durchgängig ist. Der äußere Schließmuskel bleibt also bei der Operation erhalten. Während der Operation können dann, je nach Risikokonstellation, auch die zugehörigen Lymphknoten im Becken entfernt und auf das Vorliegen von Absiedlungen untersucht werden.
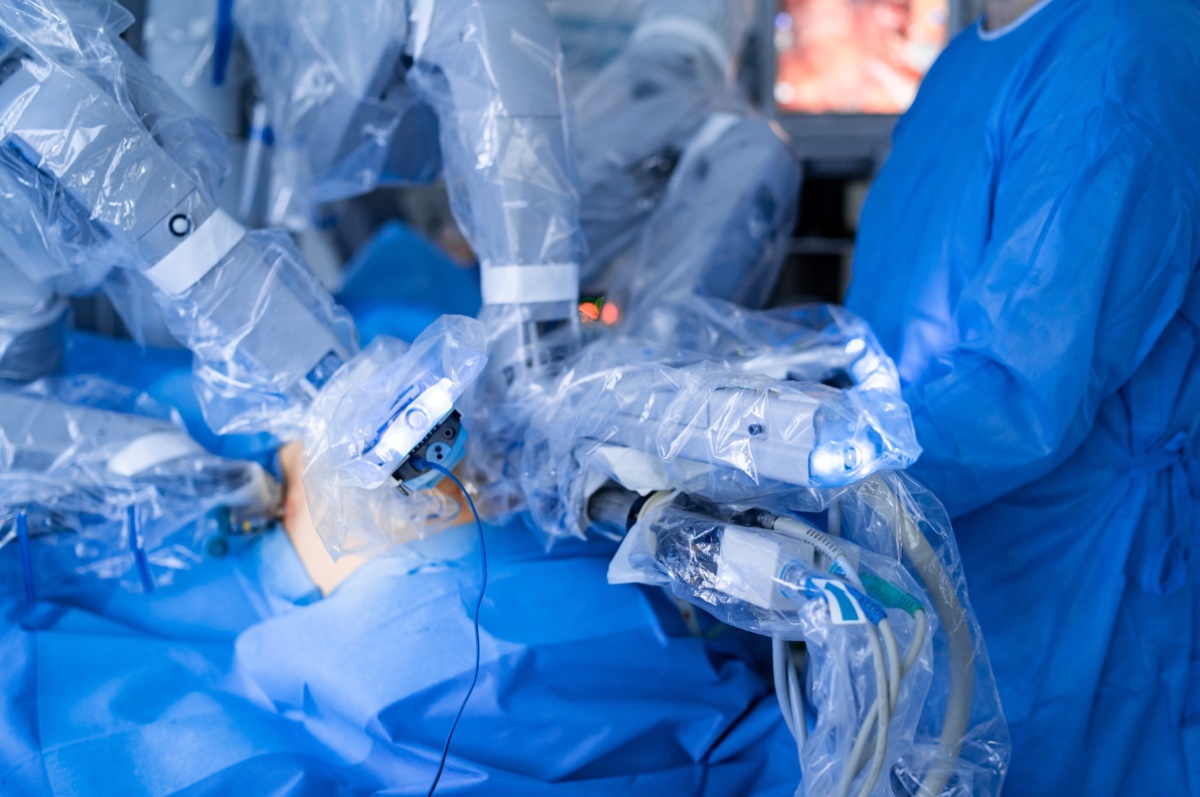
Es gibt verschiedene operative Zugangswege:
- der Eingriff kann von einem Unterbauchschnitt aus durchgeführt werden,
- ebenso laparoskopisch („Schlüsselloch-Chirurgie“) vom Bauch aus, meist mit robotischer Hilfe (z.B. DaVinci-Prostatektomie),
- und es bleibt noch der Zugang vom Damm aus (perineal).
Diese Eingriffe werden in Narkose durchgeführt und machen einen mehrtägigen stationären Aufenthalt nötig, dem sich häufig eine REHA anschließt, insbesondere zum Erlernen des Beckenbodentrainings.
Als Folge der Operation kann eine Inkontinenz aufteten, die sich in den meisten Fällen unter Beckenbodentraining weitestgehend zurückbildet. Sollte dies in Ausnahmefällen nicht der Fall sein, kann mittels operativer Methoden die Inkontinenz behandelt werden. Durch den Eingriff leidet in der Regel auch die Erektionsfähigkeit, die Gliedsteife Diese Folge kann geringer gehalten werden, wenn bei dem Eingriff das Nervengeflecht, das die Erektion steuert und in unmittelbarer Nähe der Prostata liegt, geschont werden kann (Nerverhalt), was jedoch auch eine erhöhtes Risiko für eine unvollständige Entfernung des Tumors mit sich bringt. Je nach Ausmaß der Erektionsstörung stehen verschiedenen Behandlungsoptionen nach der Operation zur Verfügung.
Nachfolgende Untersuchungen und Kontrollen:
Die bei der Operation entfernte Prostata wird vom Pathologen detailliert feingeweblich untersucht und damit werden das T-Stadium und der Gleason-Score exakt bestimmt. Gleichzeitig wird überprüft, ob der Tumor vollständig, also ohne Tumorreste im Körper, entfernt wurde (R0).
Nach 3 Monaten erfolgt die Kontrolluntersuchung beim Urologen. Der dann gemessene PSA-Wert sollte unter der Nachweisgrenze liegen.
Lesen Sie auf unserer Seite mehr zum Thema:
Strahlentherapie
Die Strahlentherapie ist eine weitere wichtige Säule in der kurativ intendierten Therapie des Prostatakarzinoms. Auch hier gibt es verschiedene Methoden:
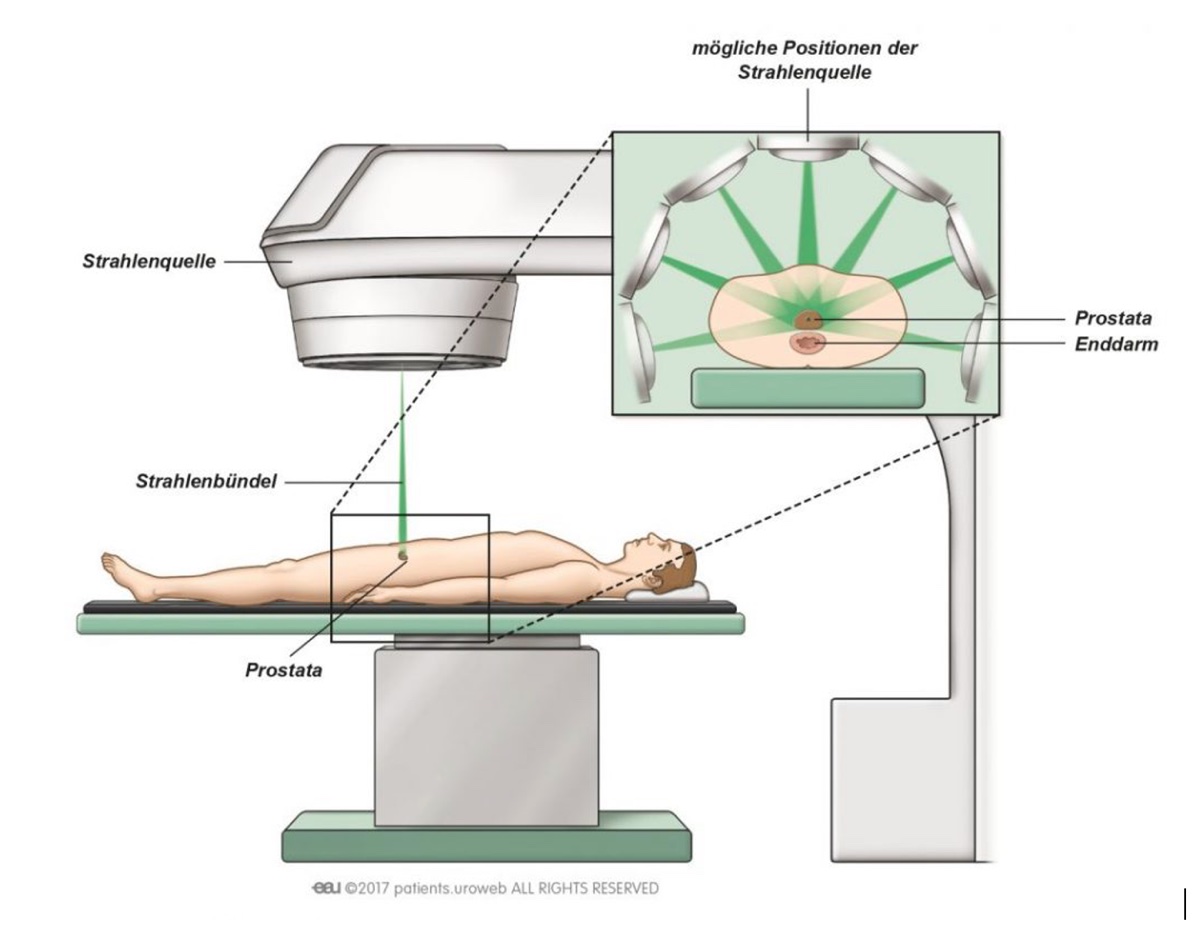
Die Perkutane Strahlentherapie ist die Bestrahlung der Prostata von außen, bei der meist arbeitstäglich über mehrere Wochen Bestrahlungen durchgeführt werden, die jeweils nur wenige Minuten dauern. Neuere Techniken können auch eine Bestrahlung der Prostata in wenigen Tagen ermöglichen. Akute Reizungen der Harnröhre und des Darmes und häufiges Wasserlassen können Folgen sein. Mittel- bis langfristig können auch hier analog zur Operation eine Inkontinenz und eine Störung der Erektionsfähigkeit auftreten.
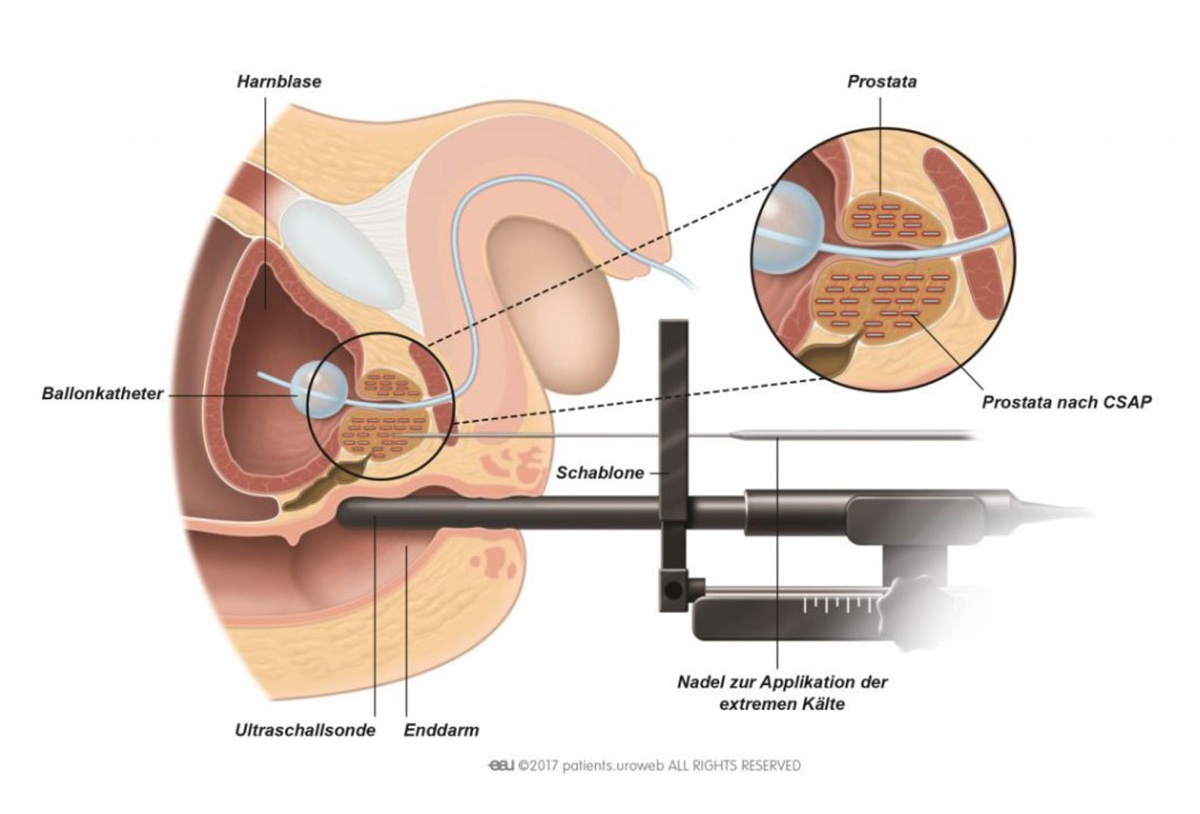
Die Brachytherapie ist die Bestrahlung von innen, bei der entweder kleine strahlende Partikel in die Prostata eingebracht werden (LDR-Brachytherapie) oder bei der die Bestrahlung durchgeführt wird über vorübergehend in die Prostata eingebrachte Nadeln (HDR-Brachytherapie), bei der eine höhere Strahlendosis möglich ist. Die Kombination mit einer Bestrahlung von außen ist möglich.
Kontrollen:
Bei der Kontrolluntersuchung etwa drei Monate nach der Strahlentherapie gibt der PSA-Wert wesentliche Informationen ebenso wie die folgenden Kontrollen. Der niedrigste Wert nach Bestrahlung wird als „Niedrigstwert“ (Nadir) in die weitere Beobachtung aufgenommen. Stiege er über die Zeit an, wäre davon auszugehen, dass der Prostatakrebs durch die Behandlung nicht vollständig geheilt wäre.
Lesen Sie auf unserer Seite mehr zum Thema:
Fokale Therapie
In den meisten Fällen gibt es mehrere Krebsherde, die über die Prostata verteilt sind und die mit Operation oder Bestrahlung der gesamten Prostata erfolgreich behandelt werden können. Sollte jedoch mit multiparametrischem Prostata-MRT und ausgedehnten Prostatabiopsien zweifelsfrei nachgewiesen werden, dass der Tumor nur an einer Stelle vorliegt oder auf eine Hälfte der Prostata begrenzt ist, kann individuell die Möglichkeit der fokalen Therapie diskutiert werden.
Dabei wird dieser Bereich beispielsweise mit hochintensivem fokussiertem Ultraschall (HIFU), Kryotherapie oder Irreversible Elektroporation (IRE behandelt. Die fokale Therapie ist im Gegensatz zu Operation und Bestrahlung kein Standard in der Behandlung des Prostatakrebses, weil ihre Ergebnisse noch nicht ausreichend erforscht sind. Nach derzeitigem Wissensstand sind fokale Therapien im Vergleich zur Standardtherapie keine gleichwertigen Behandlungsmöglichkeiten. Sie sollte nur im Rahmen kontrollierter Studien oder bei ausdrücklichem Patientenwunsch nach fundierter Aufklärung erfolgen.
Wachsames Beobachten (Watchful Waiting)
Von der aktiven Überwachung ist abzugrenzen das wachsame Beobachten (watchful waiting) bei Patienten, bei denen keine heilende Behandlung geplant ist, sondern lediglich die Symptomkontrolle mit einer medikamentösen Therapie im Fall der Befundverschlechterung. Gründe hierfür können das Patientenalter, eine besonderer Tumorkonstellationen sein oder dass der Zustand des Patienten eine heilende Therapie nicht zulässt. In diesen Fällen kann man sich auf einfachere Untersuchungen beschränken, in deren Zentrum die PSA-Kontrolle steht.
Behandlung im fortgeschrittenen Stadium
Im fortgeschrittenen Stadium ist der Prostatakrebs bereits über die Prostata hinausgegangen und hat Absiedlungen (Metastasen) gebildet, häufig in Lymphknoten und Knochen. Dies wird meist mit Skelettszintigramm, einer nuklearmedizinischen Knochendarstellung, und Computertomografiediagnostiziert oder alternativ mittels PSMA-PET-CT In dieser Krankheitsphase steht die medikamentöse Therapie im Zentrum.
Dabei sind zwei unterschiedliche Krankheitsformen voneinander abzugrenzen. Sie betreffen die Empfindlichkeit der Prostatakrebszellen gegenüber den Androgenen, den männlichen Sexualhormonen. Zu unterschieden sind das hormonsensitive (mHSPC) und das androgen-unabhängige (kastrationsresistente) Prostatakarzinom (CRPC), die jeweils unterschiedliche Behandlungsformen notwendig machen.
Das hormonsensitive Prostatakarzinom
Die zentrale Bedeutung bei dieser Therapieform hat das Testosteron. Es ist das männliche Sexualhormon, das unter Steuerung der Hirnanhangsdrüse (Hypophyse) in den Hoden gebildet wird und das Wachstum eines Prostatakrebses fördert. Über die Blutbahn gelangt es an jede Prostatakrebszelle, sowohl in der Prostata wie auch in Metastasen, und trägt dort zum Krebswachstum bei. Umgekehrt führt eine Verminderung des Einflusses des Testosterons auf die Krebszelle zu einer Rückbildung des Tumors. Dies macht man sich bei der Hormonentzugstherapie (ADT) zunutze, die die Grundlage der systemischen Therapie im fortgeschrittenen Stadium ist.
Die ADT entzieht die Prostatakrebszelle dem Einfluss des Testosterons. Es gibt bei ihr zwei unterschiedliche Verfahren, die LHRH-basierte Therapie und die Behandlung mit Antiandrogenen, von denen heute die LHRH-Therapie in den meisten Fällen die empfohlene Option darstellt In den letzten Jahren sind androgen-ähnliche Medikamente mit etwas anderem Wirkungsmechanismus hinzugekommen, die Androgenrezeptor-Signalweg-Inhibitoren, welche mit der LHRH-Therapie kombiniert werden.
LHRH-basierte Therapie
LHRH ist ein körpereigener Botenstoff, der in der Hirnanhangsdrüse dazu führt, mit einem eigenen Botenstoff in den Hoden die Bildung von Testosteron anzuregen. Dieser Vorgang kann beeinflusst werden durch LHRH-Agonisten und LHRH-Antagonisten. Mit ihrer Hilfe lässt sich die Testosteronproduktion in den Hoden unterbinden, so dass dem Prostatakrebs kein wachstumsförderndes Testosteron zur Verfügung steht. Damit wird ein Fortschreiten der Erkrankung eingedämmt, und der Tumorumfang kann sogar zurückgehen.
Die Medikamente werden üblicherweise als Depot unter die Haut oder in die Muskulatur gespritzt. Sie haben zwar kaum eigene Nebenwirkungen, doch führen sie zu den Symptomen eines Testosteron-Mangelzustandes. Dazu gehören Hitzewallungen, die Verminderung des sexuellen Verlangens (Libidoverlust) und der Erektionsfähigkeit, Gewichtszunahme, auch eine Blutarmut (Anämie).
Bedeutsam ist auch die dadurch hervorgerufene Minderung der Knochendichte, der mit der Gebe von Kalzium, Vitamin D und einer medikamentösen Knochenschutz-Therapie begegnet werden kann (Knochenprotektion). Da diese Behandlung Kieferschäden hervorrufen kann, soll vor Beginn eine zahnärztliche Untersuchung erfolgen.
Lesen Sie auf unserer Seite mehr zum Thema:
Ein vergleichbarer Effekt auf das Testosteron kann auch eine Hodenoperation erreichen, bei der das testosteronbildende Hodengewebe aus beiden Hoden ausgeschält wird (subkapsuläre Orchiektomie)
Therapie mit Antiandrogenen
Die klassischen Antiandrogene sind Medikamente, die die Wand der Prostatakrebszelle gegenüber dem Einfluss des Testosterons „versiegeln“, so dass das Testosteron keinen fördernden Einfluss auf die Zelle hat.
Diese Medikamente werden meist als Tabletten eingenommen. Zu ihren Nebenwirkungen gehören dämpfende Einflüsse auf die Sexualität, Brustdrüsenschwellungen, Stoffwechselstörungen und Bauchbeschwerden.
Therapie mit Androgenrezeptor-Signalweg-Inhibitoren
Die Androgenrezeptor-Signalweg-Inhibitoren (Apalutamid, Enzalutamid, Darolutamid, Enzealutamid) ähneln in ihrer Wirkung zwar den klassischen Antiandrogenen, haben jedoch einen anderen Wirkungsmechanismus als diese. Sie blockieren mit einem Angriff auf der Zellwand innerhalb der Krebszelle die Wachstumsimpulse, die vom Testosteron auf den Zellstoffwechsel ausgehen.
Das Medikament Abirateron, das zusammen mit Cortison eingenommen wird, vermindert die Produktion von Testosteron in anderen Organen, also nicht nur in den Hoden.
Die Medikamente werden als Tabletten eingenommen und können Müdigkeit, Gelenk- und Muskelschmerzen, Hitzewallungen, Bluthochdruck oder Verdauungsstörungen hervorrufen.
Diese Medikamente sind fester Bestandteil der Kombinationstherapien im metastasierten hormonsensitiven Stadium. In ausgewählten Fällen können sie auch bei androgen-unabhängigen Prostatakarzinomen eingesetzt werden.
Chemotherapie
Das beim Prostatakrebs gebräuchlichste Chemotherapeutikum ist Docetaxel aus der Gruppe der Taxane, kann bei fitten Patienten, speziell solche mit einer hohen Anzahl an Metastasen, als Driefachkombinationen zusammen mit LHRH-basierter Therapie und Androgenrezeptor-Signalweg-Inhibitoren eingesetzt werden.

Chemotherapeutika zerstören neben Tumorzellen die Zellen schnellwachsender Organe, also auch die der Blutbildung und des Haarwuchses. Sie führen damit auch zu entsprechenden Nebenwirkungen wie Blutbildveränderungen wie Blutarmut (Anämie), Verlust weißer Blutkörperchen mit Infektionsrisiko, Haarverlust, Verdauungsproblemen, Störungen der Fruchtbarkeit und Nervenschädigungen. Diese Nebenwirkungen können durch begleitende Medikamente gemindert werden und bilden sich meist nach Therapieende zurück.
Die Infusionen werden in regelmäßigen Abständen (Zyklen) mit Infusionen über 1 – 2 Stunden gegeben. Sorgfältige ärztliche Kontrollen während der Therapie sind notwendig.
Lesen Sie auf unserer Seite mehr zum Thema:
Das kastrationsresistente Prostatakarzinom
Im Krankheitsverlauf kann die Situation eintreten, dass der Prostatakrebs seine Empfindlichkeit für Hormontherapien verliert und diese bisher besprochenen medikamentösen Behandlungsformen nicht mehr ausreichend wirksam sind. In diesem Fall spricht man vom kastrationsresistentem Prostatakarzinom, das andere Behandlungsmethoden notwendig macht.
Chemotherapie
Im kastrationsresistenten Stadium wird die Chemotherapie ebenfalls eingesetzt, insbesondere, wenn sie im hormonsensitiven Stadium noch nicht eingesetzt wurde. Neben Docetaxel (s.o.) kann im Verlauf auch Cabazitaxel als weiteres Chemotherapeutikum eingesetzt werden.
Behandlung mit PARP-Inhibitoren
Sind Körperzellen geschädigt, versucht der Körper sie zu reparieren. Unglücklicherweise tut er dies auch, wenn es sich um Krebszellen handelt, die bei einer Krebstherapie eigentlich zerstört werden sollen. Für diese Reparatur verwendet die Zelle unter anderem einen eigenen Wirkstoff, das Enzym PARP.
Wird dieses Enzym durch ein Medikament gehemmt, misslingt die Reparatur der Krebszelle, und sie stirbt ab. Dies ist das Behandlungsprinzip bei der Therapie mit PARP-Inhibitoren, die als Tabletten gegeben wird und deren häufigste Nebenwirkungen Übelkeit, Müdigkeit und Blutbildveränderungen sind.
Diese Behandlung ist besonders gut wirksam, wenn bei dem Patienten eine spezielle Genveränderung im Tumor vorliegt, und zwar an den sogenannten HRR-Genen, die unter anderem PARP steuern Ob dies der Fall ist, lässt sich vor der Behandlung testen, indem man das Prostatakrebs-Gewebe des Patienten auf solche Veränderung untersucht. Dies geschieht entweder in den früheren Proben aus der Prostata oder in später entnommenen Metastasen-Gewebe. Damit lässt sich die Behandlung eines individuellen Patienten passgenau auf seine eigenen Besonderheiten im Erbgut ausrichten. Dies bezeichnet man als personalisierte Medizin. Es gibt jedoch auch Hinweise, dass eine gewisse Wirkung auch bei Patienten erzielt werden kann, die in der Biopsie keinen Veränderung zeigen.
Sollte eine Veränderung nachgewiesen sein, kann diese nur im Tumor (smoatische Mutation) vorliegen oder auch im gesamten Erbgut (Keimbahnmutation) des Patienten und in diesen Fällen vererbbar sein. Daher ist bei Nachweis einer Veränderung eine genetische Beratung und ggf. weitere Diagnostik zum Nachweis bzw. Ausschluss einer Keimbahnmutation zu empfehlen.
Lesen Sie auf unserer Seite mehr zum Thema:
Radioliganden-Therapie (Lutetium-PSMA-Therapie)
Die Radioliganden-Therapie ist eine besondere Form einer Bestrahlungsbehandlung, bei der die die strahlenden Substanzen den Tumor und die Krebszellen auf dem Blutweg erreichen, nachdem sie intravenös gegeben wurden. Eine weitere Besonderheit ist, dass durch diese Therapie gezielt fast ausschließlich Prostatakrebszellen bestrahlt werden bei weitgehender Schonung gesunder Zellen. Dies wird erreicht, weil die strahlende Substanz mit einem Trägerstoff verbunden wird, der eine besondere Affinität zu Prostatakrebszellen hat.
Bei dieser Behandlung wird als strahlende Substanz (Radioligand) radioaktives Lutetium mit einem speziellen Trägerstoff gekoppelt, dem sog. prostataspezifischen Membranantigen (PSMA), das im Tumor fest an die Wand der Prostata(krebs)zellen andockt. Dies stellt sicher, dass diese Substanz die Zielstruktur Prostatakrebszelle identifiziert und ausgewählt. Damit wird die strahlende Substanz Lutetium fest an die Zelle gebunden und kann sie zerstören. Daraus resultiert eine sehr zielgerichtete Behandlung der Tumorzelle unter weitgehender Schonung gesunden Gewebes.
Diese Behandlung hat in der Regel ihren Platz, wenn von Hormon- oder Chemotherapie keine Verbesserungen mehr zu erwarten sind. Ob sie erfolgreich durchgeführt werden kann, lässt sich zuvor am besten bildgebend mit einem PSMA-PET-CT beurteilen. Die Therapie erfolgt in mehreren Sitzungen über mehrere Wochen. Zu ihren Nebenwirkungen zählen Müdigkeit, Übelkeit, Veränderungen im Blutbild und ein verstärkter Speichelfluss
Lesen Sie auf unserer Seite mehr zum Thema:
Bestrahlung von Knochenmetastasen
Fortschreitende Prostatakrebse können Metastasen in den Knochen bilden und tun dies häufig in der Wirbelsäule. Sie führen nicht nur zu Schmerzen, sondern zerstören die Knochensubstanz mit der Gefahr von Knochenbrüchen. Knochenmetastasen können im Skelettszintigramm erkannt werden, bei dem in die Vene gespritzte strahlende Substanzen die Knochen und Strukturauffälligkeiten darstellen. Ebenso in der Computertomografie (CT), einer Schnittbilduntersuchung des Körpers, die durch gezielte Röntgenuntersuchungen ergänzt werden kann.
Wenn es sich um einzelne Metastasen handelt, können diese Knochenmetastasen gezielt von außen bestrahlt werden. Diese Bestrahlung vermindert Schmerzen, stabilisiert den Knochen und senkt damit die Gefahr eines Knochenbruchs. Dazu sind mehrere Sitzungen der Strahlentherapie nötig, die meist gut vertragen wird.
Entscheidungsfindung in der Prostatakrebsbehandlung
In früheren Jahren waren das Wissen über den Prostatakrebs und seine verschiedenen Erscheinungsformen geringer und das therapeutische Arsenal kleiner. Zu diesen Zeiten konnte der Urologe vor Ort weitgehend alleine über das Vorgehen beraten. Heute ist das Wissen immens gewachsen, und es stehen sehr viele Behandlungsmöglichkeiten zur Verfügung, die abhängig von der jeweiligen Tumorausprägung stadiengerecht eingesetzt werden müssen. Zeitgleich gibt es viele Studien mit neuen Erkenntnissen zu einzelnen Aspekten der Erkrankung, die weltweit auf großen Krebskongressen vorgestellt und dann in der Literatur veröffentlicht werden. Daran sind nicht nur Urologen, sondern auch Onkologen und Strahlentherapeuten beteiligt. Dieses neue Wissen, das nach diesen Kongressen schnell vor Ort umgesetzt werden soll, können am besten einzelne Spezialisten überblicken, die detaillierte Kenntnisse und große Erfahrung in dieser Erkrankung haben.
Um dieses immense Wissen jedem einzelnen Patienten zukommen zu lassen und seine Behandlung zeitnah auf die neuesten Erkenntnisse abzustimmen, wurden flächendeckend Tumorkonferenzen (Tumorboards) eingerichtet. In ihnen beraten Spezialisten aus der Urologie, der Onkologie, der Strahlentherapie und evtl. weiterer Fächer gemeinsam über jeden einzelnen Patienten und erarbeiten für ihn anhand des Krankheitsverlaufs Vorschläge für das weitere Vorgehen. Für den Patienten bleiben sein Urologe oder seine Urologin vor Ort jedoch weiter der vertraute Ansprechpartner.
Wichtige Entscheidungskriterien für solche Entscheidungen sind das aktuelle Wissen über:
- Gleason-Score: der bei der feingeweblichen Untersuchung durch den Pathologen gefundene Gleason-Score gibt wesentliche Auskünfte über die biologischen Eigenschaften des Prostatakrebses, insbesondere über seine Aggressivität und Wachstumstendenz.
- PSA-Wert: er gibt Informationen über die augenblickliche Aktivität des Tumors und erlaubt den Vergleich mit früheren und zukünftigen Werten gibt Hinweise für Verbesserung oder Verschlechterung
- PSA-Verdoppelungszeit: dabei wird bestimmt, innerhalb welchen Zeitraums sich der PSA-Wert auf das Doppelte seines ursprünglichen Wertes erhöht hat. Dieser Zeitraum erlaubt zeitliche Aussagen über die zukünftige Entwicklung des Prostatakrebses.
- Tumorstadium: Angaben über das T-, N- und M-Stadium, nach einer Operation auch über das R-Stadium (Vollständigkeit der Tumorentfernung)
- Metastasierungsmuster: Die Anzahl und die Lokalisation vorliegender Metastasen bestimmen maßgeblich die individuelle Auswahl der (Erst-)Therapie.
- Hormonempfindlichkeit: für die Auswahl der geeigneten medikamentösen Therapieform ist es wichtig zu wissen, ob das Prostatakarzinom hormonsensibel ist, also ob es auf eine Hormonentzugstherapie anspricht, oder ob es als homonrefraktär auf bestimmte Behandlungen nicht ansprechen wird.
- Bisherige Behandlungen: Gerade beim fortgeschrittenen Prostatakrebs ist die Reihenfolge von Therapien nicht beliebig, sondern muss sorgfältig abgestimmt werden auf die bisher schon durchgeführten Behandlungen.
- Körperlicher Zustand des Patienten: daran entscheidet sich, welche Form der Therapie einem Patienten zugemutet werden kann.
Psychoonkologische Betreuung
Eine Krebserkrankung und ihre Behandlung stellen einen Patienten und seine Angehörigen vor erhebliche psychische Belastungen, die sie in vielen Fällen allein schlecht stemmen können. Hier ist Hilfe möglich durch Psychoonkologen, also Psychotherapeuten, die sich auf die Betreuung krebskranker Patienten spezialisiert haben. Patienten und ihre Angehörigen können nur ermuntert werden, diese Hilfe in Anspruch zu nehmen.
Prävention von Prostatakrebs
Zur Prävention von Prostatakrebsraten raten Urologen und Urologinnen zu:
- Gesunder Ernährung mit dem Schwerpunkt auf pflanzlichen Produkten
- Normalgewicht
- Ausreichender Bewegung
- Maßvollem Alkoholgenuss
- Rauchverzicht.
